
Las autoridades británicas afirman que la vacuna está lista, que su uso es seguro y que cumplieron con todos los pasos del proceso para garantizarlo. De hecho, el país planea empezar a vacunar a partir del próximo 7 de diciembre.

Jamás una vacuna había tardado tan poco tiempo en ser desarrollada y autorizada para uso público.
Este miércoles, 10 meses después de desatarse la pandemia, Reino Unido aprobó la vacuna de Pfizer y BioNTech contra el coronavirus.
Fue el primer país del mundo en dar ese paso, aunque se espera que otros organismos tomen decisiones al respecto pronto.
En Estados Unidos, la Administración de Alimentos y Medicamentos (FDA) decidirá si aprobar o no la vacuna a partir del 10 de diciembre. Su homóloga en Europa, la Agencia Europea del Medicamento (EMA), lo tiene previsto el 29 de este mismo mes.
Tras el anuncio de Reino Unido, la Unión Europea (UE) defendió su cautela, asegurando que su proceso se basa en un análisis de evidencia más exhaustivo que el de Reino Unido, en una línea similar a lo expresado por las autoridades sanitarias de EE.UU.
"Reino Unido no lo ha hecho tan cuidadosamente como nosotros", defendió Anthony Fauci, científico jefe del equipo especial contra el coronavirus de la Casa Blanca, en declaraciones a la cadena Fox News.
Pero las autoridades británicas afirman que la vacuna está lista, que su uso es seguro y que cumplieron con todos los pasos del proceso para garantizarlo. De hecho, el país planea empezar a vacunar a partir del próximo 7 de diciembre.
Mientras el mundo mira atento a la primera campaña nacional de vacunación contra el covid-19, surgen varios interrogantes.
¿Por qué Reino Unido tomó esta decisión antes que cualquiera? ¿Qué tan rápido lograrán la inmunidad los británicos?
Aquí se responde a estas y otras preguntas.
1. ¿Por qué Reino Unido aprobó la vacuna antes que la Unión Europea o Estados Unidos?
El ministro de Sanidad británico, Matt Hancock, asegura que el Brexit -la salida de Reino Unido de la UE- facilitó la decisión.
Pero Reino Unido sigue acogiéndose a las regulaciones de la EMA hasta el final del período de transición, que culmina el próximo 1 de enero.
La legislación europea sostiene que las vacunas las autoriza la EMA, pero recoge que cualquier país puede solicitar un procedimiento de emergencia que les permita distribuirlas temporalmente en su mercado interno.

June Rain, jefa ejecutiva del regulador de medicamentos británico, aseguró que autorizaron la vacuna bajo la ley europea.
La doctora June Raine, jefa ejecutiva de la Agencia Reguladora de Medicamentos y Productos Sanitarios de Reino Unido (MHRA, por sus siglas en inglés), dijo este miércoles que "autorizaron el suministro de la vacuna bajo la ley europea, vigente hasta el próximo 1 de enero".
Raine aseguró que el trabajo de la MHRA británica se corresponde con "los estándares internacionales" y que, a pesar de ser los primeros en aprobar la vacuna, no se han saltado ningún paso.
"Nuestra rapidez o progreso se basó completamente en la disponibilidad de datos durante nuestra evaluación periódica, y en una revisión rigurosa y el asesoramiento independiente que recibimos", dijo el miércoles.
2. ¿Se apresuró Reino Unido en su decisión como dice Fauci?
En medio de la difícil situación por la que pasan múltiples países a causa de la pandemia y los beneficios de empezar con la vacunación, políticos de otros países salieron a defender su mayor cautela y algunos científicos, como Anthony Fauci, en EE.UU., llegaron a considerar que Londres se había apresurado.
Reino Unido "realmente se precipitó con su aprobación", manifestó Fauci, director del Instituto Nacional de Alergias y Enfermedades Infecciosas de EE.UU., en declaraciones a la cadena CBS.
"La manera en que funciona la FDA, la manera en que lo está haciendo, es la correcta", defendió el experto en otra entrevista en Fox News.
"La idea no es ser el primero sino tener una vacuna segura y efectiva", dijo por su parte el ministro de Sanidad de Alemania, Jens Spahn, en una conferencia de prensa.
La EMA europea explicó en un comunicado que usaba un método más lento que Reino Unido para aprobar las vacunas y consideró que su procedimiento es el "mecanismo más apropiado en la actual emergencia por la pandemia".

La vacuna de Pfizer/BioNTech se desarrolló en apenas 10 meses.
Como explica la corresponsal en asuntos de Salud de la BBC Naomi Grimley, el mecanismo de la FDA sí es "diferente al de otros organismos del mundo".
"Suele pedir a los fabricantes de vacunas su información en bruto y dedica tiempo volviéndola a analizar", señala Grimely.
El organismo en Londres, por su parte, "se basa más en los informes de las propias empresas como ocurre con la EMA europea, con sede en Ámsterdam".
No obstante, la política puede también explicar por qué la FDA no había dado luz verde, señala la corresponsal.
"En octubre, el presidente Trump presionó a las autoridades sanitarias para aprobar las primeras candidatas a vacunas antes del día de las elecciones (3 de noviembre), pero se resistieron a ello, temiendo que pudiera politizarse".
La FDA fijo que quería revisar datos adicionales sobre la fase final de los ensayos antes de que las farmacéuticas pudieran recibir una aprobación de emergencia.
"Inevitablemente eso hizo que algunos argumentaran que EE.UU. se había visto envuelto en una revisión más detallada que la necesaria".
Sin embargo, funcionarios de Reino Unido estiman que tanto Washington como Bruselas darán su aprobación pronto, señala la periodista.
3. ¿Cuáles pueden ser los efectos secundarios de la vacuna y por qué Reino Unido defiende que es segura?
La mayoría de los efectos adversos de la vacuna de Pfizer y BioNTech son leves, similares a los de otras vacunas y normalmente no duran más de un día, de acuerdo al profesor Munir Pirmohamed, presidente de la Comisión de Medicina Humana en Reino Unido.
Estos pueden incluir dolores musculares y leve subida de la temperatura.

La rapidez con la que Reino Unido aprobó la vacuna ha sido cuestionada sutilmente por la Unión Europea.
La vacuna de Pfizer ha demostrado un 95% de efectividad en todos los grupos de edad analizados, incluyendo ancianos.
La británica MHRA, con gran reputación internacional, ha estado revisando datos preliminares sobre los ensayos de la vacuna desde junio y aseguró que el proceso de aprobación fue exhaustivo.
"Ninguna vacuna sería autorizada para su distribución en Reino Unido a menos que se cumplan los estándares esperados en seguridad, calidad y eficacia", subrayaron desde el organismo.
4. ¿Quiénes serán los primeros en vacunarse?
De forma similar a otros países con planes de vacunación, Reino Unido priorizará ciertos grupos de población.
Primero serán los ancianos en residencias y sus cuidadores, luego los mayores de 80 años y el personal sanitario y a partir de ahí se irá vacunando a todos los grupos de edad mayores de 50.

Jonathan Van-Tam, asesor médico del gobierno británico, aclaró que las medidas de protección continuarán hasta asegurarse que la vacunación está reduciendo los casos de coronavirus.
También se priorizará a aquellos que entre 16 y 64 años estén en grupos de riesgo por padecer dolencias previas.
El doctor Simon Stevens, jefe ejecutivo del servicio nacional de salud británico, confía en que la vacunación del primer grupo se complete en diciembre.
Según el Comité Conjunto de Vacunación e Inmunización de Reino Unido, los grupos prioritarios incluyen el 90-99% de población de mayor riesgo.
A mayor edad, más probabilidades de enfermar de gravedad o morir por el virus. Dicho riesgo incrementa considerablemente a partir de los 70 años. Las personas con dolencias previas también son más vulnerables, señalan los expertos.
Tras la fase inicial, que incluye nueve grupos distintos, se iniciará una segunda fase de vacunación para más jóvenes.
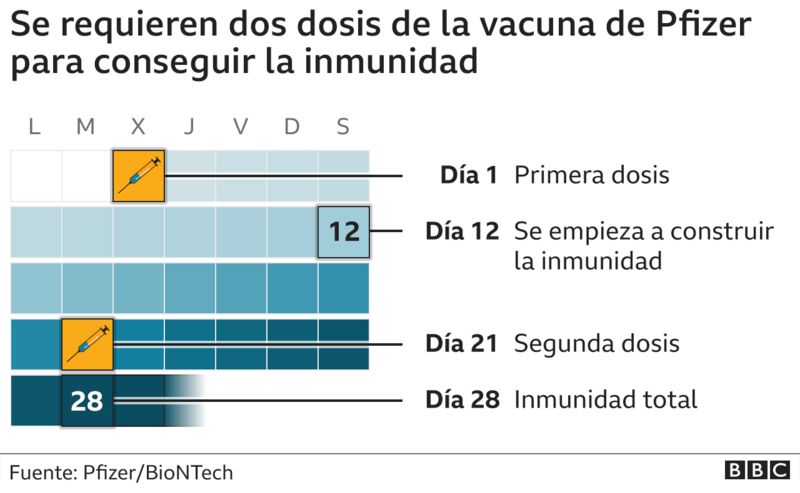
5. ¿Qué tan rápido se logra la inmunidad con la vacuna de Pfizer y BioNTech?
En total, alrededor de un mes.
El compuesto de Pfizer y BioNTech se administra en dos dosis separadas por 21 días y la inmunidad total no se consigue hasta alrededor de una semana después de la segunda dosis, según explicó Jonathan Van-Tam, asesor médico del gobierno británico.
Pero de acuerdo al especialista, "tampoco puede asegurarse una protección total en cada persona. Dependerá de cada caso", explicó a BBC Radio 5.
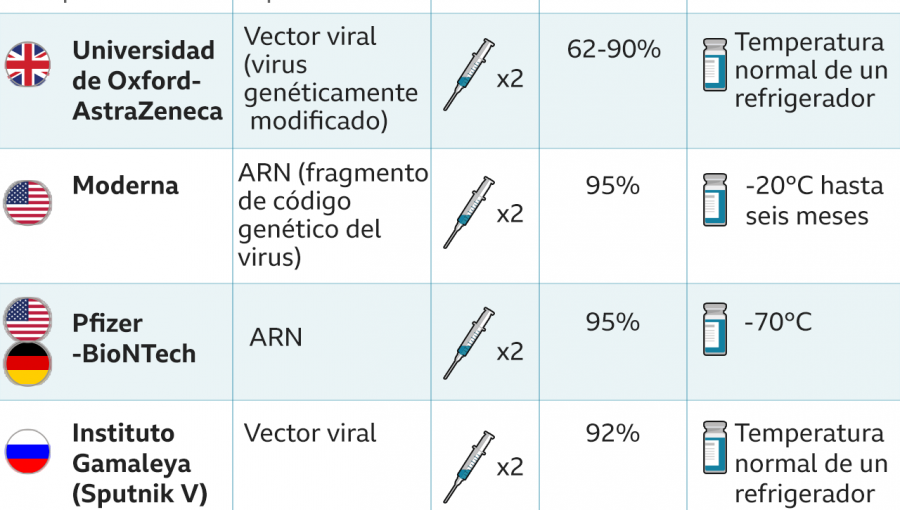
Otras vacunas pendientes de aprobación también requieren dos dosis, como la de Moderna y la de la Universidad de Oxford y AstraZeneca.
6. ¿Cuánto tiempo durarán las restricciones una vez comience la vacunación?
Reino Unido acaba de culminar su segundo confinamiento nacional. Ahora impuso un sistema de niveles de restricciones según la incidencia del virus en cada región del país.
Pero comenzar a vacunar no significa el fin de estas medidas.
"Hasta que no comprobemos que la vacuna esté funcionando y que los números están cayendo, es muy probable que continúen las restricciones de protección durante un tiempo. Necesitamos estar muy seguros antes de decir a la gente que puede relajarse", dijo Van-Tam en una conferencia de prensa el miércoles.
Los ensayos clínicos de Pfizer y otros fabricantes de vacunas han demostrado proteger a las personas de enfermar de gravedad por el nuevo coronavirus, pero todavía se desconoce si también detienen la transmisión.

Por otra parte, expertos consultados por BBC Mundo señalan que para empezar a hablar de una supuesta normalidad, primero debe alcanzarse un 70% de inmunidad poblacional.
Algunas predicciones en Reino Unido o España, por ejemplo, esperan conseguir dichos porcentajes entre la primavera y el verano de 2021.
Pero los expertos advierten que para volver a la completa normalidad, los porcentajes deben darse en toda la población mundial. Esto puede tomar varios meses e incluso años, especialmente en los países con menos recursos o en vías de desarrollo.
PURANOTICIA // BBC MUNDO